下列推断正确的是
A.SiO2是酸性氧化物,能与NaOH溶液反应
B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是()。
A、根据氧化物的元素组成,将氧化物分为酸性氧化物和碱性氧化物
B、根据溶液导电能力的强弱,将电解质分为强电解质和弱电解质
C、根据是否具有丁达尔效应,将分散系分为溶液和胶体
D、根据化学反应中物质焓值的变化,将化学反应分为放热反应和吸热反应
A.SiO2、FeO
B.TiO2、Fe2O3
C.SiO2、NiO2、FeO
D.SiO2、TiO2、Fe2O3
SiO2俗称石英砂,是光导纤维的主要成分,下列关于SiO2的有关叙述正确的是()。
A.SiO2是酸性氧化物,它不溶于水也不溶于任何酸
B.SiO2是制造玻璃的主要原料之一,它在常温下不与NaOH溶液反应
C.因高温时SiO2与Na2CO3反应放出CO2,所以H2SiO3酸性比H2CO3强
D.CO2通入水玻璃中可得原硅酸
下列氧化物以下说法不正确的是()
A、酸性氧化物都是非金属氧化物,
B、碱性氧化物都是金属氧化物,但金属氧化物不一定碱性氧化物。
C、酸性氧化物都是酸酐,都含有相对应的含氧酸,但不一定都能与水反应。
D、离子型氧化物都是强电解质,共价型氧化物都是非电解质
二氧化硫和氮的氧化物是大气的主要污染物,防止和治理环境污染是当前环保工作的重要研究内容之一。 (1)一定条件下,2SO2(g)+O2(g)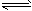 2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和 0.2mol SO3(g),2min后反应达到平衡时,测得SO2的转化率为50%,则该可逆反应的平衡常数K= ___;恒温下,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率_____50%(选填“>”、“<”或“=”)。 (2)用CH4催化还原NOx为N2可以消除氮氧化物的污染。现有1L NO2、NO混合气体NOx,将其还原成 N2,需同温同压下CH4的体积0.4L,则混合气体中NO2、NO的物质量之比为_____。 (3)新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示
2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和 0.2mol SO3(g),2min后反应达到平衡时,测得SO2的转化率为50%,则该可逆反应的平衡常数K= ___;恒温下,若往容器中再加入2 mol SO2(g),则重新达到平衡时SO2的总转化率_____50%(选填“>”、“<”或“=”)。 (2)用CH4催化还原NOx为N2可以消除氮氧化物的污染。现有1L NO2、NO混合气体NOx,将其还原成 N2,需同温同压下CH4的体积0.4L,则混合气体中NO2、NO的物质量之比为_____。 (3)新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中的酸性氧化物分解除去,转化流程如图所示
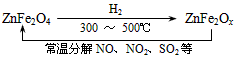
若2mol ZnFe2Ox与SO2可生成0.75 mol S,x=_____。求可分解⑵中混合气体体积V(标准状况下)。(写出计算过程)