某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道: NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 。 【提出问题】能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢? 【实验验证】如图是该学习小组进行模拟实验时所用到的部分主要装置。已知浓氨水遇生石灰会产生大量的NH3。
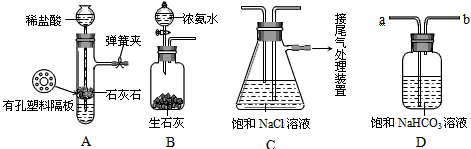
请回答下列问题: ⑴ 检验A装置气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若 ,说明装置不漏气。 ⑵ D是连接在装置A与装置C之间的气体净化装置,进气口是 (填a或b),D的作用是除去______气体。 ⑶ 实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是______。(填写序号) ① 使CO2更易被吸收 ② NH3比CO2更易制取 ③ CO2的密度比NH3大 ⑷ 用________的方法将生成的NaHCO3晶体从混合物中分离出来。 【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3。
A.侯氏制碱法的工艺过程中应用了物质溶解度的差异
B.可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
C.碘是人体必需微量元素,所以要多吃含高碘酸的食物
D.黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成
我国著名化学家侯德榜发明的联合制碱法的主要原理是:向浓氨水中通入足量的CO2生成NH4HCO3(碳酸氢铵),然后加入食盐充分搅拌,两者发生复分解反应,由于碳酸氢钠的溶解度很小,便呈晶体析出,将析出的碳酸氢钠加热得碳酸钠,二氧化碳和水.
(1)请写出上述原理的三个化学方程式:
①______;
②______;
③______.
(2)有人认为侯氏制碱法有以下优点,你认为正确的是______.
A.生产过程中部分产物可作为原料使用 B. 副产品是一种氮肥 C.反应不需要加热,可节约能源.
1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
①NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3②2NaHCO3=Na2CO3+H2O+CO2↑
(1)在反应①中,生成的氯化铵和碳酸氢钠的质量比是53.5:______.
(2)如图为碳酸氢钠和氯化铵的溶解度曲线,30℃时,碳酸氢钠饱和溶液中的溶质质量分数______(填“大于”、“等于”或“小于”)氯化铵饱和溶液中的溶质质量分数.
(3)氨盐水吸收CO2后生成了碳酸氢钠和氯化铵,请你根据溶解度曲线和生成物质量关系分析:为何碳酸氢钠首先结晶析出?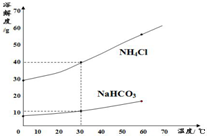
我国制碱工业先驱--侯德榜先生发明的侯氏制碱法的主要原理是:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl.关于这一反应的说法正确的是()
A.该反应属于化合反应
B.该反应属于复分解反应
C.反应的各元素存在化合价变化
D.该反应能进行是因为NaHCO3溶解度较小