以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
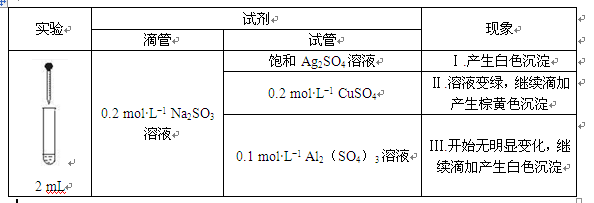
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42?,含有Cu+、Cu2+和SO32?。
已知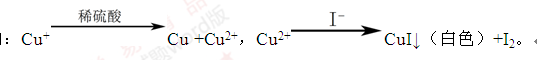
①用稀硫酸证实沉淀中含有Cu+的实验现象是_________。
②通过下列实验证实,沉淀中含有Cu2+和SO32?。
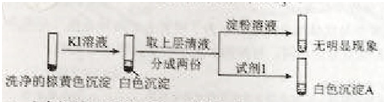
a.白色沉淀A是BaSO4,试剂1是________。
b.证实沉淀中含有Cu+和SO32?的理由是_______。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42?,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.呗Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。

步骤二:_________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有____\_。盐溶液间反应的多样性与__________有关。
水中亚硫酸钠过剩量愈高,亚硫酸钠与氧的反应速度愈快。所以水中亚硫酸钠过剩量愈高愈好。()
A、对
B、错
植物吸收SO2以后,便形成亚硫酸及亚硫酸盐,然后又以一定的速度将亚硫酸氧化成()。
碘量法测定酒精中醛的含量,下面有关解释不正确的是()。
A.用亚硫酸氢钠与醛起加成反应
B.用碘来氧化过量的亚硫酸氢钠
C.加入少量碳酸氢钠,调节溶液PH值
D.用碘滴定从与醛结合中游离出来的亚硫酸氢钠
亚硫酸钠除氧的原理是根据()。
A.亚硫酸钠能够降低氧在水中的溶解度
B.气体溶解定律
C.使溶解氧进入锅炉之前与亚硫酸钠发生反应而消耗
D.提高锅水温度,使溶解氧逸出