1879年,日本明治天皇在《教学大旨》中说,“文明开化”后,“破品行,伤风败俗者不少。”“其流弊在于后仁义忠孝,徒洋风是竞。将来之所恐,终至不知君臣爷子大义。”并指令“自今以往,基于祖宗之训典,专明仁孝忠义。道德之学,以孔子为主,人人尚诚实之品行。”上述材料表明,当时的日本政府
A.决意复活儒学道德
B.准备放弃文明开化
C.强力推行欧化政策
D.鼓励移植西方技术
造成东北地区冬季漫长严寒的主要原因是①邻近冬季风源地②海拔高③纬度较高④千岛寒流影响
A.①②③
B.①③④
C.②③④
D.①③
明治维新为日本资本主义经济迅速发展提供的条件主要是①统一国内市场 ②自由劳动力 ③技术和人才 ④资金
A.①②③
B.②③④
C.①③④
D.①②③④
(15分)甲醇是一种非常好的燃料。熔点-97.8°C,沸点64.5°C。一定条件下,CO与H2反应可制得甲醇:CO+2H2 CH3OH
CH3OH
图1表示该反应进行过程中的能量变化;
图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。 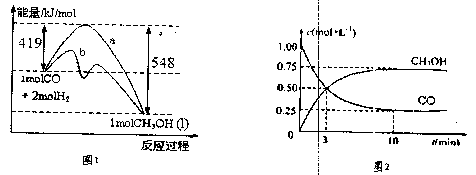
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,写出表示CH3OH燃烧热的热化学方程式 。
(2)根据上图2计算:该温度下,反应CO(g)+2H(g) CH3OH(g)的平衡常数为 10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
CH3OH(g)的平衡常数为 10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
A.降低温度 B.加催化剂
C.充入氩气,使体系压强增大 D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压
(3)已知:CH3OH可以在一定条件下转化为HCOOH,HCOOH和CH3COOH性质相似。25°C,0.1mol/L的HCOOH溶液的pH>1。室温下,向0.1mol/L的HCOOH中加NaOH。
①当溶液中离子浓度关系满足c(HCOO-)
C.NaOH过量
②若加入过量的NaOH,在加入NaOH的过程中,H2O的电离程度如何变? 。
CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。其中一种途径是将CO2转化成有机物实现碳循环。此反应达平衡时平衡常数为: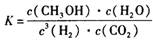 且温度升高,K值变小。下列说法正确的是
且温度升高,K值变小。下列说法正确的是
A.该反应的化学方程式为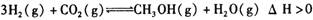
B.在恒温、恒容的密闭容器中,若混合气体的密度不再改变时,该反应一定达到平衡状态
C.平衡时,其他条件不变,使用催化剂有利用于CO2的转化
D.在恒温、恒容的密闭容器中,增大H2的浓度时,CO2的转化率增大
读“我国东南沿海某地地形剖面图”,回答下列问题。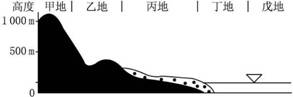 (1)填表:将下列选项的字母填入相应的空格内(每空填一项):
(1)填表:将下列选项的字母填入相应的空格内(每空填一项):
甲地
乙地
丙地
丁地
戊地
适宜的农业生产方式
A.水产养殖与捕捞 B.发展林木业
C.果树栽培 D.捕捞生产E.种植业 F.放牧业(2)如果采用不合理的利用方式,可能会发生水土流失的地方是______\_地;可能会产生沙化现象的地方是____________地。(3)为了减少灾害和保护环境,在沿海地带应__________林。