(13分)工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂
亚氯酸钠(NaClO2),其工艺流程如下:
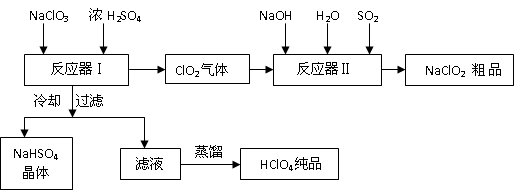
已知:
1.NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
2.高氯酸是至今为止人们已知酸中的最强酸,沸点90℃。
请回答下列问题
(1)反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是 。
(2)反应器Ⅱ中发生反应的离子方程式为 。
(3)通入反应器Ⅱ中的SO2用另一物质H2O2代替同样能生成 NaClO2,请简要说明双氧水在反应中能代替SO2的原因是
(4)Ca(ClO)2、ClO2、NaClO、NaClO2等含氯化合物都是常用的消毒剂和漂白剂是因为它们都具有 请写出工业上用氯气和NaOH溶液生产另一种消毒剂 NaClO的离子方程式
AP/AN/O工艺()。
A.是同步除磷脱氮工艺
B.污水首先进入厌氧反应器,回流的含磷污泥在这里充分释放磷
C.第二个反应器是缺氧反应器,主要功能是生物反硝化,有从第三个反应器——好氧反应器的出水回流进入
D.第三个反应器是好氧反应器,同时具有降解BOD和除磷的功能,但不能发生硝化反应